Cafeína
Martes 15 - Abril - 2014
Uso de cafeína en
neonatos : Indicaciones, farmacocinética, efectos clínicos y
resultados
Nicole R. Dobson NeoReviews Vol.14 No.11 November 2013
Traducción literal : Dr Gerardo Flores Henríquez
Introducción
Los primeros estudios que
documentan la eficacia de las metilxantinas ( aminofilina , teofilina,
cafeína) para la apnea del prematuro ( AOP ) se publicaron hace más de
30 ańos. (1) Los efectos clínicos de estas metilxantinas son
equivalentes y la cafeína actualmente ha sustituído en gran medida la
aminofilina y la teofilina para el tratamiento de rutina debido a su
índice terapéutico más amplio y mayor vida media que permite la
administración una vez al día . (2) El uso exclusivo de cafeína en
RN de muy bajo peso al nacer (MBPN) aumentó de 26 % de todo el uso de metilxantinas en 1997 a 96% en 2010 . (3) La cafeína es ahora uno de
los fármacos más comúnmente prescritos en UCIN y ha sido descrita apropiadamente como una " bala de plata " en
la
neonatología. (1)
Varias revisiones de la
terapia con cafeína en recién nacidos se han publicado
recientemente. (1) (2) Datos recientes indican que el inicio del
tratamiento con cafeína antes de una edad postnatal de 3 días puede tener
efectos beneficiosos adicionales sobre los outcomes más tardíos y que
dosis de mantención más altas pueden estar asociadas con beneficios
adicionales sin efectos adversos . Esta revisión de la utilización de
cafeína proporciona una actualización de conocimientos actuales ,
con énfasis en (1) mecanismos de acción, (2) propiedades
farmacológicas , ( 3 ) efectos clínicos y seguridad , ( 4 )
dosis de mantenimiento óptima y ( 5 ) efectos sobre outcomes clínicos
más tardíos.
Mecanismos de acción
Actuando tanto central
como periféricamente , las metilxantinas estimulan los centros respiratorios
medulares , aumentan la sensibilidad al dióxido de carbono , inducen broncodilatación y mejoran la función diafragmática , lo que lleva a
un aumento de la ventilación minuto , respiración mejorada y menor
depresión respiratoria hipóxica. ( 2 ) ( 4 ) En los prematuros ,
teofilina aumenta el volumen corriente debido a un aumento en trabajo
inspiratorio. ( 2 ) Otros efectos de las metilxantinas incluyen la
estimulación de los sistemas nervioso central y cardiovascular , aumento
de la secreción de catecolaminas , aumento de la diuresis y
antagonismo de la actividad de prostaglandina. ( 2 )
La cafeína es una trimetilxantina que ejerce principalmente sus efectos
mediante el bloqueo de los receptores de adenosina A1 y A2A . El bloqueo de
los receptores de adenosina causa importantes efectos secundarios sobre
muchas clases de neurotransmisores , incluyendo noradrenalina ,
dopamina , serotonina , acetilcolina , glutamina y ácido gammaaminobutírico
. ( 5 )
Los receptores de adenosina están presentes en cerebro, corazón ,
vasos sanguíneos , rińones , tracto gastrointestinal y
sistema respiratorio . Estudios recientes sugieren que el principal
mecanismo por el cual las metilxantinas reducen la apnea es a través del
antagonismo de los receptores A2A en las neuronas GABAérgicas . ( 6 )
( 7 ) El efecto de la cafeína sobre los quimiorreceptores del cuerpo carotídeo es menos claro , pero puede ser excitatorio durante el
desarrollo temprano mediante el bloqueo de los receptores de adenosina
A1 ubicados en nervios que inervan el cuerpo carotídeo y causan mayor
trabajo respiratorio. ( 8 ) Interesantemente, los
polimorfismos del gen del receptor de adenosina afectan la susceptibilidad a
apnea del prematuro (AOP) y
pueden explicar la variabilidad individual de la respuesta a cafeína .
( 9 )
Fármacocinética
La cafeína se metaboliza
en el hígado y las enzimas responsables de su metabolismo maduran
progresivamente con el aumento de edad gestacional al nacer y edad
postmenstrual (PMA) en aumento. (2) El proceso de N7-desmetilación es la
principal vía metabólica de la cafeína en nińos prematuros y las nińas tienen una mayor
tasa de metabolismo de cafeína que los nińos. (2) Hay cuatro
isoformas del citocromo P450, incluyendo las isoformas del citocromo P450
de la subfamilia CYP2C, que contribuyen al metabolismo de la cafeína en
el hígado. (10) La 7-N-desmetilación es catalizada de forma no
específica, principalmente por el CYP1A2 y en menor medida, por CYP2C8
/ 9 y CYP3A4. A concentraciones más altas de cafeína, la contribución de
CYP1A2 disminuye en favor de CYP2C8 / 9.
Datos de la farmacocinética de la
cafeína son limitados en los neonatos con MBPN . ( 11 ) El clearance en
nacidos prematuros es marcadamente más bajo y el volumen de
distribución es más alto que a la edad equivalente al término y más allá. (
12 ) En prematuros nacidos a una edad gestacional media de 29
semanas y recibiendo citrato de cafeína a dosis de 6 mg / kg /día por vía intravenosa, el
rango de percentil 25 a percentil 75 de las
concentraciones séricas fue de 18 a 23 mg / l en los primeros 14 días
después del parto . A esta edad, las concentraciones de cafeína sérica no dependían de la PMA , peso
ó edad postnatal y se
mantuvieron en un rango seguro y terapéutico sobre los rangos de las
funciones renales y hepáticas encontradas típicamente en la
práctica. ( 11 )
En prematuros nacidos a las 24 a 29 semanas de gestación y peso al nacer de
570 a 1.570 g semanas , la cafeína oral se absorbe por completo .
El clearance aumentó de forma no lineal con la edad postnatal en aumento , mientras
que el volumen de distribución se incrementó linealmente con el aumento
de peso. ( 12 ) La media de la vida media de eliminación fue de 101 horas.
La eliminación de cafeína estaba disminuída inicialmente en nińos
extremadamente prematuros y luego aumentó linealmente hasta la
evaluación final a las 6 semanas . Sin embargo , el clearance disminuído no
se explica
totalmente por el peso corporal y factores de
desarrollo relacionados con el tiempo tuvieron un efecto importante en la
eliminación de la cafeína , según lo indica un impacto significativo de la
edad postnatal.
En otros estudios de prematuros que
reciben tratamiento de rutina con cafeína , el clearance aumentó
con la edad gestacional al nacer en aumento y peso actual y edad
postnatal más altos , sobre todo en la gestación de más de 28 semanas. ( 2 ) No se
identificaron factores clínicos que influenciaran el volumen de
distribución . Entre todos los nińos estudiados , el clearance (L / d
) = 0,14 x Peso ( kg ) + 0.0024 x edad posnatal ( días ) (±
20 %) y
volumen de distribución = 0,82 L (±
24 %).
Dosis y niveles de cafeína
La dosificación de rutina de citrato de cafeína ha sido una dosis de carga de 20 mg / kg ( 10 mg / kg de cafeína base ), seguida de una dosis de mantenimiento diaria de 5 mg / kg. ( 11 ) La aprobación original por la Food and Drug Administration de cafeína para tratamiento de AOP se basó en este régimen de dosificación . Sin embargo, algunos estudios han reportado el uso de dosis de mantención más altas de 15 a 30 mg / kg / día. ( 2 ) ( 13 ) En un estudio reciente , una dosis de mantenimiento diaria de 20 mg / kg de citrato de cafeína desde el período de periextubación fue tan bien tolerada como la dosis de comparación de 5 mg / kg / día . ( 14 ) ( 15 ) La mayoría de los centros de neonatología de Estados Unidos ahora utilizan dosis de mantenimiento de 5 a 8 mg / kg y en ocasiones de hasta 10 mg / kg por día de citrato de cafeína para la terapia de rutina durante las primeras semanas después del parto (Tabla 1 ) .
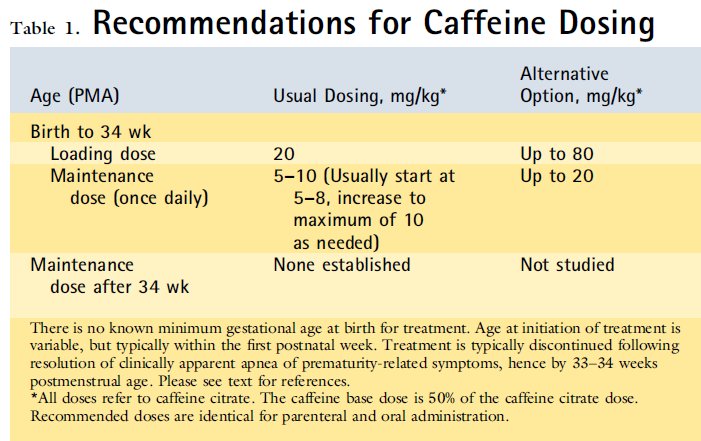
Algunos centros internacionales
utilizan dosis de mantenimiento de citrato de cafeína de hasta 20 mg / kg
por día, pero dosis de mantenimiento superiores a 10 mg / kg por día
son raras en las UCIN de EE.UU. El tratamiento suele ser suspendido
a las 33 -
34 semanas de EPM (edad postmenstrual) , después de la resolución de los síntomas clínicamente
aparentes relacionados con la AOP . Algunos centros continúan la cafeína
más allá de 34 semanas PMA , aunque poca evidencia apoya la eficacia de esta
práctica.
Los
prematuros en edades postmenstruales más jóvenes parecen tolerar en
forma segura concentraciones de cafeína de hasta 50 a 84 mg / L. ( 2 ) ( 13
) Dosis de mantenimiento de cafeína de rutina suelen ser suficientes
para alcanzar concentraciones sanguíneas de 8 a 20 mg / L en neonatos
de menos de 32 semanas de EPM. Después de 32 semanas de EPM ,
sin embargo, y especialmente en > 33 semanas , los niveles disminuirán
progresivamente debido al aumento de metabolismo de la cafeína a menos
que se aumente la dosis mg / kg . Sin embargo , no hay datos más allá de
33 a 34 semanas de EPM para establecer la dosis de mantenimiento de
cafeína necesaria para alcanzar un nivel sanguíneo terapéutico.
Debido a que el clearance de cafeína aumenta progresivamente con el aumento de PMA , a la misma dosis de mantenimiento por kilogramo en el menor de 34 semanas , los niveles de cafeína a las 36 semanas de EPM probablemente sólo serán aproximadamente la mitad de los niveles obtenidos a las 32 semanas de EPM . ( 12 )
La medición de rutina de los niveles séricos de cafeína no se ha demostrado que sea necesario. ( 11 ) ( 16 ) En un estudio con una mediana de dosis de mantenimiento de 5 mg / kg por día a una mediana de edad gestacional de 28 semanas , la mayoría de los niveles de cafeína en plasma estuvieron entre 5 y 20 mg / L , independiente de la edad gestacional , nitrógeno ureico en sangre , creatinina sérica ó niveles de enzimas hepáticas. ( 17 )
Beneficios terapéuticos
Aunque la cafeína es más
comúnmente utilizada en UCIN para tratar los síntomas relacionados con AOP y
para facilitar la extubación (Tabla 2 ) , hay beneficios adicionales de
la terapia. El estudio Cafeína para Apnea de la Prematuridad (CAP) , un
gran estudio clínico , randomizado, proporciona los datos más recientes y
completos con respecto a cafeína y morbilidades neonatal . ( 18 ) (
19 ) ( 20 )

El estudio CAP se realizó desde 1999 a 2004 y randomizó 2.006
nińos con peso 500 a 1.250 g a cafeína ó placebo dentro de los
primeros 10 días de vida y el tratamiento se continuó hasta que la
terapia ya no era clínicamente necesaria. El grupo de cafeína recibió
una dosis de carga de 20 mg / kg de citrato de cafeína y una dosis de
mantenimiento inicial de 5 mg / kg por día . La mediana de edad al
inicio del tratamiento fue de 3 días ( rango intercuartil [ IQR ] 2-5) ,
la duración media del tratamiento fue 37 días ( IQR 24-46 ) y la
mediana de la PMA a la última dosis fue de 34,4 semanas (IQR 33.0 - 35.9 )
. ( 19 ) Los resultados específicos del estudio CAP se resumen en las
siguientes secciones.
Apnea de prematuridad
Los síntomas relacionados con
apnea ocurren en hasta 85% de los prematuros nacidos con menos de 34 semanas
de gestación. (2) La revisión Cochrane de seis
estudios que evalúan el uso de metilxantinas (tres estudios de
cafeína) concluyó que metilxantinas son eficaces para reducir la
frecuencia de los eventos de apnea y el uso de ventilación
mecánica. (21) La cafeína tiene un riesgo relativo de fracaso del
tratamiento de 0,46 (intervalo de confianza del 95% [IC], 0,27-0,78).
(22) El estudio CAP, ya descrito, no fue diseńado para
evaluar directamente la eficacia de la cafeína para tratamiento de
síntomas relacionados con apnea, pero el análisis post hoc mostró que
los neonatos tratados con cafeína para prevenir ó tratar los síntomas
relacionados con apnea tuvieron mejores outcomes clínicos. (19) (20)
(23)
La asociación de cafeína con mejores outcomes (resultados) en combinación con su
mejor perfil de seguridad llevó a los revisores de Cochrane a la
conclusión de que la cafeína es la "droga preferida" para el tratamiento
de AOP. (21)
Varios estudios han
evaluado la eficacia de cafeína como profilaxis para prevenir
síntomas relacionados con apnea . Dos estudios, que randomizaron
un total de 104 recién nacidos a cafeína ó placebo , no encontraron
diferencias en el número de nińos que presentan apnea , bradicardia y
eventos hipoxémicos , ó en el uso de ventilación con presión positiva .
( 24 ) Sin embargo , estos estudios se basaron en el reporte de apneas
junto a la cuna/incubadora del paciente y técnicas de monitoreo menos sofisticadas
para definir eventos hipoxémicos . Un estudio reciente que comparó
cafeína y teofilina mostró que la profilaxis con cafeína parecía
controlar la apnea en recién nacidos en riesgo , inicialmente no
sintomáticos , pero después de la primera semana de tratamiento , los
beneficios de cafeína y teofilina eran comparables. (16)
Aunque la actual revisión Cochrane concluye que la evidencia disponible no apoya el uso de cafeína como profilaxis para prevenir la apnea , el estudio CAP y los otros beneficios de la terapia temprana con cafeína con riesgo mínimo , como se analiza más adelante en este artículo, justifica el uso de profilaxis temprana con cafeína en nińos prematuros. ( 24 )
Apnea postoperatoria
Los nińos nacidos
prematuramente, especialmente aquellos con historia de AOP ó enfermedad
pulmonar crónica, tienen mayor riesgo para la apnea postoperatoria,
desaturación de oxígeno unido a hemoglobina y bradicardia después de administración de anestesia general. (25)
Varios pequeńos estudios
clínicos de administración de cafeína a dosis de 5 a 10 mg / kg
durante ó inmediatamente después de la inducción anestésica
revelaron una disminución en la apnea postoperatoria. (26) Dado que la
cafeína tiene efectos adversos mínimos a estas dosis, la cafeína a
menudo se administra a prematuros para prevenir la apnea
postoperatoria después de la anestesia general.
Síntomas relacionados con apnea en otras condiciones clínicas
La terapia con cafeína se ha
utilizado para manejar otras formas de apnea y síntomas
relacionados en neonatos. La apnea asociada a Arnold-Chiari se ha tratado
con éxito con cafeína. (27)
Además, la cafeína puede desempeńar un rol en el manejo de los neonatos con bronquiolitis viral, incluyendo su desarrollo secundario a infección por el virus sincicial respiratorio. Los nińos pequeńos con bronquiolitis tienen un riesgo significativo de apnea, especialmente si nace prematuramente. Varias pequeńas series de casos han reportado reducción de la apnea relacionada a bronquiolitis con la administración de cafeína, (28), pero ésto no se ha estudiado en el contexto de un estudio controlado randomizado.
Al igual que en resultados anteriores con teofilina, la cafeína también se ha utilizado con éxito para corregir síntomas relacionados con apnea más tardía en nińos en riesgo de, ó que ya han experimentado, un evento aparente que amenaza la vida (Alte) que requiere intervención. (29)
Extubación
La revisión Cochrane de
los efectos del tratamiento profiláctico con metilxantinas para
facilitar el weaning de ventilación mecánica y extubación
concluyó que el tratamiento causa una reducción
significativa en el fracaso de extubación dentro de 1 semana (riesgo
relativo 0,48 , 95 % IC : 0,32 a 0,71 ) . ( 30 ) El estudio CAP
no reportó directamente tasas de éxito de extubación, pero el grupo de
cafeína tenía PMAs (edades postmenstruales) más jóvenes al final del uso de terapia de
oxígeno , ventilación con presión positiva e intubación endotraqueal. ( 19 )
Un estudio randomizado, doble ciego de 3 diferentes regímenes de
dosis de mantenimiento de citrato de cafeína (3, 15 , y 30 mg / kg )
para manejo periextubación de 127 nińos nacidos con menos de 32 semanas
de gestación no mostró diferencias en fracaso de
extubación entre los grupos , pero los neonatos en los 2 grupos de dosis
más altas tuvieron significativamente menos apnea documentada en
comparación con el grupo de dosis más bajo . ( 13 )
Otro estudio de los mismos investigadores que compararon regímenes de dosis de mantenimiento de 20 y 5 mg / kg por día de citrato de cafeína para manejo periextubation mostró una reducción significativa en el fracaso de extubación en el grupo de dosis alta (riesgo relativo 0,51, IC del 95%: 0,31 -0,85 ) . ( 15 ) Además, en el subgrupo de neonatos con una edad gestacional menor de 28 semanas al nacer , la duración de la ventilación mecánica fue significativamente menor en el grupo de dosis alta. No se observaron aumentos de efectos adversos de la dosis más alta y no se observaron efectos adversos a más largo plazo en el primer ańo de vida. ( 14 ) ( 15 )
Los mecanismos para la mejora de las tasas de éxito de extubación no se comprenden bien . Un estudio reciente en recién nacidos prematuros que evaluó la función muscular respiratoria mostró mejoras en la capacidad residual funcional , presiones máximas generadas durante oclusiones al final de inspiración y espiración y compliance y disminución de la resistencia del sistema respiratorio después de administración de cafeína. ( 31 ) Estos resultados sugieren que la cafeína mejora la fuerza de los músculos respiratorios , lo cual puede facilitar el weaning de la ventilación mecánica .
Función pulmonar y Displasia broncopulmonar
La cafeína mejora la
función pulmonar aumentando el impulso respiratorio central y la
actividad del diafragma , así como mediante la inducción de diuresis
y broncodilatación. En los babuinos nacidos prematuramente con
síndrome de dificultad respiratoria , la terapia temprana con cafeína en
combinación con surfactante redujo la resistencia de la vía aérea y mejoró la distensibilidad pulmonar ,
el índice de
eficiencia ventilatoria y la relación arterial / alveolar de pO2 en las
primeras 24 horas después del nacimiento . ( 32 ) Un estudio reciente en
prematuros mostró que la cafeína mejora la fuerza muscular
respiratoria . ( 31 ) En el estudio CAP , el tratamiento con cafeína se
asoció en promedio con 1 semana menos de intubación endotraqueal ,
ventilación con presión positiva y uso de oxígeno suplementario y menos
uso de corticoides postnatales . ( 19 )
Además , las tasas de displasia broncopulmonar (DBP ) fueron significativamente inferiores en el grupo cafeína en comparación con el grupo placebo ( 36,3 % frente a 46,9 % ; odds ratio ajustado, 0,63 , P < 0,001 ) . ( 19 ) Es de destacar que los beneficios de la cafeína eran más significativos cuando el tratamiento se inició en los primeros 3 días después del nacimiento . ( 23 ) Este beneficio también ha sido evidente en dos estudios de cohortes retrospectivos recientes en los que terapia con cafeína en primeros 3 días de edad se asoció con aproximadamente la mitad de la incidencia de DBP en comparación con el inicio más tardío de la terapia . ( 3 ) ( 33 )
Hipoxia intermitente
Hipoxia intermitente (IH)
se define como breves ciclos repetitivos de disminución de la
saturación de hemoglobina a partir de una línea de base de normoxia
seguidos por reoxigenación y regreso a normoxia. IH ocurre comúnmente
en los prematuros, pero los datos que confirman el significado
clínico de IH en recién nacidos y lactantes son
limitados. Existe una asociación entre IH y severidad de la
retinopatía del prematuro. (34) Evaluaciones más tardías del
outcome del neurodesarrollo han mostrado deficiencias asociadas
con disminuciones recurrentes frecuentes en la saturación de oxígeno de
la hemoglobina a la edad de término equivalente y en la primera
infancia. (35) (36)
En un estudio reciente de recién nacidos prematuros cercanos al alta de UCIN, la cafeína redujo significativamente el número de episodios de IH, especialmente en neonatos de 35 a 36 semanas de EPM. (37) Si la duración extendida del tratamiento con cafeína en nińos de MBPN a la edad equivalente al término, tiene efectos adversos posteriores ó cualquier mejora de beneficios a largo plazo debida a disminución en la extensión de IH requiere más estudio.
Efectos cardiovasculares y Ductus arterioso
persistente
Las metilxantinas
aumentan la frecuencia cardiaca, la variabilidad del ritmo cardíaco,
volumen sistólico y la presión arterial . ( 38 ) En adultos , la
tolerancia a los efectos cardiovasculares de la cafeína por lo general
se desarrolla dentro de unos pocos días , pero no se sabe si el mismo
fenómeno ocurre en nińos prematuros . La frecuencia cardíaca por sí sola
no puede ser usada para predecir niveles tóxicos del fármaco y
niveles altos del medicamento no necesariamente causan taquicardia. ( 2
) En el estudio CAP, los recién nacidos en el grupo de cafeína
requirieron menos intervención para cierre del CAP en comparación
con los neonatos en grupo placebo ( 29 % versus 38 %, p < 0,001 ; odds
ratio ajustado 0,67). ( 19 ) Sólo el 4,5 % de los
recién nacidos en el grupo de la cafeína requirieron ligadura del DAP en
comparación con 12.6 % en el grupo placebo ( P < 0,001 ; odds ratio
ajustado 0,32) . ( 19 ) Dos estudios retrospectivos encontraron que
la terapia precoz con cafeína dentro de los primeros 3 días de vida se
asoció con un menor número de bebés que requirieran tratamiento para DAP
en comparación con el inicio tardío de la terapia. ( 3 ) ( 33 )
Los efectos beneficiosos de la cafeína en el cierre del CAP pueden estar relacionados con una mayor diuresis y el antagonismo de la actividad de prostaglandinas . ( 2 )
Efectos sobre Sistema nervioso central
y outcomes del neurodesarrollo
La adenosina es crítica
para mantener los niveles de ATP , especialmente en el cerebro . Durante
la hipoxia e inflamación, los niveles de adenosina en el tejido
cerebral aumentan dramáticamente . La adenosina protege el cerebro
durante la lesión hipóxico-isquémica experimental en modelos animales
y la activación de los receptores A1 de adenosina protege contra injuria excitotóxica (glutamato ). ( 2 )
Por tanto se debiera esperar que la
administración aguda de cafeína pudiera interferir con los efectos neuroprotectores normales de la adenosina y en modelos animales , la
exposición a corto plazo a cafeína a menudo altera los procesos de
desarrollo y empeora la lesión neuronal . ( 2 ) ( 39 )
La administración crónica de cafeína, sin embargo , parece tener un efecto neuroprotector , presumiblemente por regulación hacia arriba de los receptores de adenosina A1 . ( 40 ) En crías de ratón P3- P12 (equivalentes al tercer trimestre del embarazo humano ) , la activación del receptor de adenosina A1 contribuyó a la disminución inducida por hipoxia de la mielinización cerebral y ventrículomegalia. ( 41 ) El tratamiento con cafeína atenuó los efectos de la hipoxia , presumiblemente a través de bloqueo de los receptores de adenosina A1. ( 42 ) Además, la cafeína altera la morfología de las sinapsis neuronales y aumentó el tamańo de las espinas dendríticas . ( 43 )
La cafeína es un
excitante generalizado del sistema nervioso central. Los efectos
neurológicos agudos de administración de metilxantina incluyen nerviosismo,
temblores e hipertonía. (2) Varios estudios pequeńos que evalúan la
estructura del sueńo en prematuros han arrojado resultados
contradictorios sobre el efecto de la cafeína sobre en la organización del
sueńo. (44) (45) En un estudio reciente en nińos prematuros, las amplitudes
de la electroencefalografía de amplitud integrada aumentaron después de la
administración de cafeína, pero las implicaciones clínicas de este
aumento de la actividad de corteza cerebral son desconocidos. (46)
El efecto de la cafeína
sobre la hemodinamia cerebral ha sido evaluado extensivamente. Varios
estudios han demostrado reducciones en el flujo sanguíneo cerebral
después de la administración de cafeína , ( 47 ) (48) aunque otros
estudios no han encontrado tal efecto . ( 49 ) En el estudio CAP , las
tasas de hemorragia intraventricular y leucomalacia periventricular
no difirieron entre los grupos tratados con cafeína y placebo. ( 19 ) Los
primeros estudios sugirieron que el tratamiento con cafeína en la UCIN
no se asociaba con outcomes adversos a largo plazo . ( 2 ) El estudio CAP
reportó que la terapia de cafeína desde una mediana de edad de 3 días hasta las
34 semanas de EPM (edad post menstrual) en neonatos que pesan menos de 1.250 g al nacer reduce la
probabilidad de muerte , discapacidad clínica ó deterioro neurocognitivo
a los 18 meses de EPM.
El outcome primario de muerte ó sobrevida con discapacidad del neurodesarrollo importante se produjo en 40,2 % de los recién nacidos en el grupo cafeína en comparación con 46,2 % de los nińos asignados al grupo placebo (odds ratio ajustado , 0,77 ; p = 0,008 ) . ( 20 ) El seguimiento posterior de los nińos del estudio CAP a los 5 ańos no reveló ninguna diferencia en el outcome compuesto de muerte ó deterioro severo , pero hubo mejoría estadísticamente significativa en la coordinación motora y la percepción visual en el grupo tratado con cafeína.
Además, estas mejorías en la función motora se asociaron con un mejor desarrollo microestructural de materia blanca cerebral en la imagen de resonancia magnética a la edad de término equivalente. (50) El estudio CAP no fue diseńado para evaluar los mecanismos de las mejoras observadas en el neurodesarrollo más tardío. Sin embargo, los beneficios neuroprotectores observados de la cafeína posiblemente podrían estar relacionados con una menor incidencia y severidad de IH debido a sus efectos estimulantes respiratorios y / o para dirigir los mecanismos neuroprotectores.
Retinopatía de Prematuridad
En el estudio CAP,
la retinopatía severa del prematuro ocurrió en 5,1% del grupo
tratado con cafeína versus 7,9% del grupo placebo (odds
ratio ajustado 0,61, IC del 95%: 0,42 a 0,89). (20) Los autores
especularon que la reducción en la retinopatía severa del prematuro se
debe a duración más corta de la presión positiva de vía aérea y
oxígeno suplementario. Además, hipoxia intermitente se
ha asociado con retinopatía severa del prematuro y se ha reportado que
la cafeína disminuye la extensión de la hipoxia intermitente. (34) (37)
Otros efectos
Consumo de O2 y crecimiento
Los nińos nacidos a
las 28 a 33 semanas de gestación y tratados con cafeína tenían
consumo de oxígeno y gasto de energía aumentado durante un período de 4 semanas
y la ganancia diaria de peso fue significativamente menor en comparación
con un grupo control. (2) El estudio CAP encontró efectos similares
sobre la ganancia de peso inicialmente, con los RN tratados con
cafeína aumentando significativamente menos de peso durante las 3 primeras
semanas después de la randomización. (19) Sin embargo, a las 4 semanas después de
randomización no hubo diferencia en la ganancia de peso
y a los 18 a 21 meses, las medias de percentiles para peso, talla y
circunferencia cefálica no fue diferente entre los nińos en los
grupos de cafeína y placebo. (20) En un estudio que comparó dosis de
mantención de citrato de cafeína
de 5 y 20 mg / kg por día, los nińos
randomizados a dosis más alta requirieron más tiempo para recuperar
el peso al nacer, pero la diferencia de la media fué sólo 1,9 días (14,8 vs 12,9 días). (15)
Efectos renales
Las metilxantinas
inducen
diuresis a través del aumento del flujo sanguíneo renal y de la
filtración glomerular. Estudios posteriores en recién nacidos prematuros
confirmaron el efecto diurético de la cafeína y también revelan un
aumento significativo en el clearance de creatinina y excreción
urinaria de calcio. La cafeína no afecta las concentraciones séricas de sodio, potasio,
calcio ó fósforo. (2)
Efectos gastrointestinales: reflujo y
enterocolitis necrotizante
Las metilxantinas pueden
empeorar el reflujo gastroesofágico (GER) mediante el aumento de las
secreciones gástricas y relajación del tono del esfínter esofágico inferior
por la mejoría de niveles de AMP cíclico intracelular. (2) En los
estudios realizados a finales de 1980, aproximadamente la mitad de los
recién nacidos tratados con metilxantinas mostró aumento en el
tiempo de reflujo durante el monitoreo del pH esofágico que era
independiente de la concentración plasmática de xantina y se resolvió
después de suspender la terapia. (2) Estos estudios fisiológicos generaron
preocupación entre algunos neonatólogos. Sin embargo, los síntomas
atribuíbles a GER son comunes en los prematuros y se correlacionan
pobremente con GER demostrado. Ningún estudio ha demostrado un
empeoramiento de los síntomas de RGE relacionados con el tratamiento de
cafeína.
Varios estudios han
documentado una reducción en las velocidades de flujo sanguíneo
mesentérico en recién nacidos prematuros después de la administración de
una dosis de carga de 25 a 50 mg / kg de citrato de cafeína. (2) (47)
Sin embargo, un estudio reciente utilizando una dosis de carga de 10 mg/
kg de cafeína base (equivalente a 20 mg / kg de citrato de cafeína) no
reveló cambios significativos en las velocidades de flujo de arteria
mesentérica superior. (51) Un estudio de terapia con cafeína para
apnea en recién nacidos prematuros reportó una tendencia hacia más enterocolitis necrotizante
en el grupo de cafeína en comparación con el grupo placebo, aunque no
fue estadísticamente significativa. (22)
Sin embargo, en el estudio CAP, la incidencia de enterocolitis necrotizante fue similar en ambos grupos: 6,3% en grupo cafeína en comparación con 6,7% en grupo placebo (p = 0,63; odds ratio ajustada 0,93). (19) Del mismo modo, la incidencia de enterocolitis necrotizante no aumentó con una dosis de mantenimiento de 20 mg / kg por día de citrato de cafeína en comparación con 5 mg / kg por día. (15)
Inflamación
Los receptores de
adenosina se expresan en las células inmunes. Se ha demostrado que la terapia
con cafeína modula las funciones celulares inmunes in vitro por
antagonismo del receptor de adenosina. (52)
Un estudio reciente en
prematuros nacidos con < 31 semanas de gestación reportó que el
tratamiento con cafeína induce cambios en el perfil de citoquinas. (53)
Los niveles de cafeína dentro del rango terapéutico de 10 a 20 mg / L
estaban asociados con un perfil anti-inflamatorio (concentraciones
disminuídas de interleuquina-6 y de factor de necrosis tumoral -
α
, concentraciones
aumentadas de interleucina-10), mientras que los
niveles de cafeína sobre 20 mg / L estaban asociados con un perfil proinflamatorio. (53) Este perfil
de citoquina antiinflamatorio puede
contribuir a la menor incidencia de DBP observado en neonatos tratados con cafeína en
estudio CAP, (19) pero las
implicaciones clínicas del perfil proinflamatorio en niveles más
altos de cafeína son desconocidos y no están asociados con ninguna
consecuencia adversa conocida.
Efectos adversos y toxicidad
El estudio CAP no
reveló ningún efecto adverso significativo a corto y largo plazo de la
terapia con cafeína en UCIN. (18) (19) (20) reportes de casos
de sobredosis accidental de cafeína en prematuros han descrito
diversas alteraciones neurológica, cardiovascular y metabólicas agudas.(54)
Los síntomas neurológicos asociados con una sobredosis incluyen
agitación, irritabilidad, temblor, opistótonos e hipertonía, así como
tambien movimientos tónico - clónicos y
movimientos de labios equivalentes a actividad convulsiva.
Los signos cardiorrespiratorios de toxicidad de cafeína incluyen taquicardia
y taquipnea.
Costo - Efectividad
Un análisis económico del
estudio CAP mostró que la terapia de cafeína es costo - efectiva en prematuros. (55) En comparación con el tratamiento con placebo, el
costo promedio por nińo se redujo en $ 9,039 (dólares canadienses) en el
grupo de cafeína y el análisis de costo-efectividad mostró que la
cafeína es una terapia dominante ó ganadora. Los neonatos tratados con
cafeína tuvieron al mismo tiempo mejores outcomes y costos promedio más
bajos.
Conclusiones
La cafeína se utiliza ampliamente en la UCIN para tratar ó prevenir los síntomas relacionados con la apnea y facilitar el weaning de ventilación mecánica. Datos publicados documentan que la cafeína es segura, costo - efectiva , tiene importantes beneficios para los prematuros y es bien tolerada en todas las dosis utilizadas .
En base a los resultados positivos del estudio CAP, sin evidencia de dańo, los nińos de MBPN deben recibir rutinariamente terapia con cafeína , en particular, si el peso al nacer es inferior a 1.250 g . Es importante destacar que evidencia emergente sugiere que la terapia con cafeína precoz iniciada antes de los 3 días de vida puede mejorar los outcomes neonatales en comparación con el inicio más tardío, pero estos hallazgos necesitan ser validados en estudios prospectivos randomizados de profilaxis con cafeína .
Los niveles de cafeína no requieren ser obtenidos como parte del manejo clínico de rutina. El tratamiento clínico de rutina con cafeína suele ser discontinuado ó suspendido a las 33 - 34 semanas de EPM , trás el cese de los síntomas relacionados con apnea. La seguridad a largo plazo y eficacia del tratamiento con cafeína extendido más allá de la edad en que la apnea sintomática se ha resuelto y la dosis óptima a usar , no se conocen en este momento , pero merecen estudio adicional.